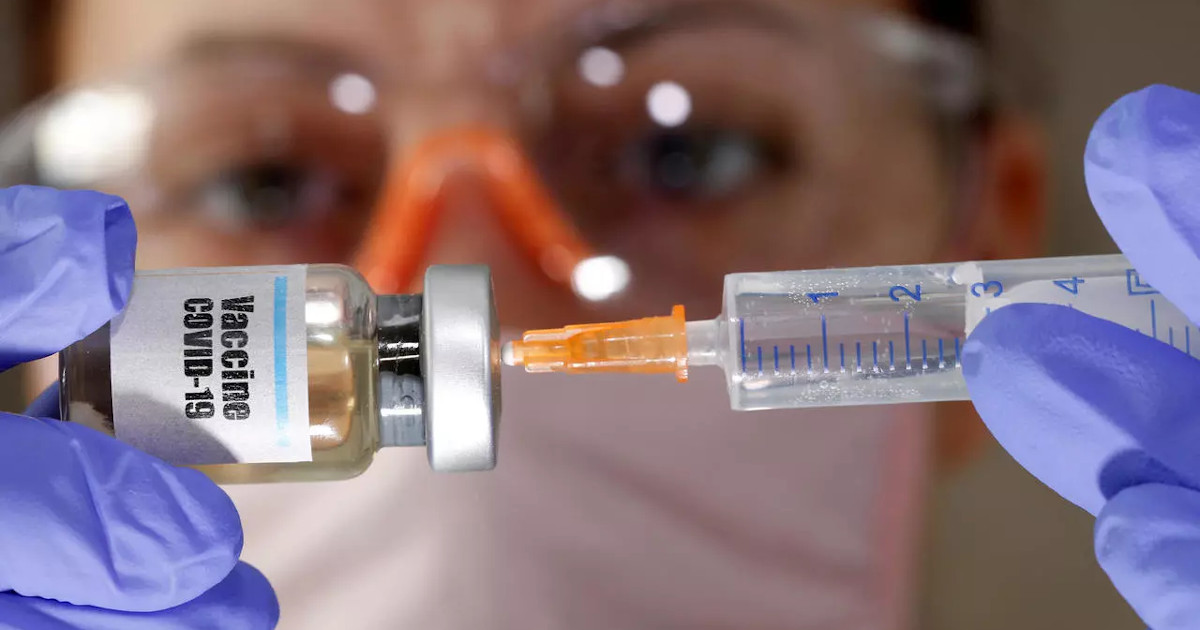
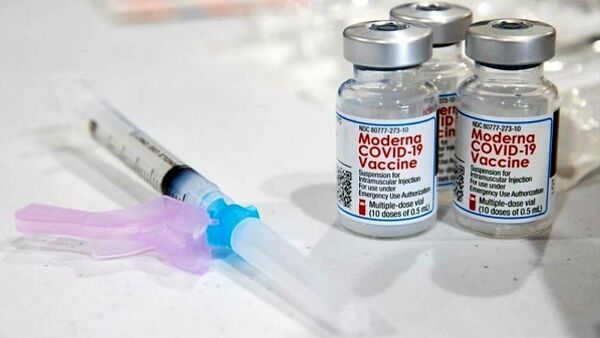
Bruxelles – Era atteso per settembre il parere del comitato per i medicinali per uso umano dell’Ema e al primo del mese il via libera è arrivata la raccomandazione per l’autorizzazione di due vaccini adattati per “fornire una protezione più ampia contro il Covid-19”, colpendo la variante Omicron BA.1. Si tratta di Comirnaty Original/Omicron BA.1 e Spikevax Bivalent Original/Omicron BA.1, sviluppati rispettivamente da Pfizer/BioNTech e da Moderna.
Come si legge nella nota pubblicata oggi dall’Agenzia europea per i medicinali, “i vaccini vengono adattati – cioè aggiornati – per adattarsi meglio alle varianti circolanti del Sars-CoV-2”, con la previsione di “mantenere una protezione ottimale contro il Covid-19 con l’evoluzione del virus”. Gli studi hanno dimostrato che i due vaccini adattati da Pfizer/BioNTech e da Moderna “sono in grado di innescare forti risposte immunitarie” contro la variante Omicron BA.1 e il ceppo originale di Sars-CoV-2 “in persone precedentemente vaccinate“, mentre gli effetti collaterali sono “paragonabili a quelli osservati con i vaccini originali, in genere lievi e di breve durata”. Allo stesso tempo, i vaccini originali Comirnaty e Spikevax “sono ancora efficaci nel prevenire la malattia grave, l’ospedalizzazione e la morte associate al Covid-19” e “continueranno a essere utilizzati nelle campagne di vaccinazione nell’Ue, in particolare per le vaccinazioni primarie”, sottolinea l’Ema.
I due pareri sui vaccini adattati alla variante Omicron saranno ora inviati alla Commissione Europea, che dovrà adottare la decisione finale. Dopodiché saranno le autorità nazionali degli Stati membri a stabilire chi deve ricevere quali vaccini e quando, “tenendo conto di fattori quali i tassi di infezione e di ospedalizzazione, il rischio per le popolazioni vulnerabili, la copertura vaccinale e la disponibilità dei vaccini”, avverte comitato per i medicinali per uso umano dell’Agenzia. Con l’evolversi della pandemia, la strategia dell’Unione rimane quella di disporre di un’ampia gamma di vaccini adattati che mirano a diverse varianti di Sars-CoV-2, in modo da fornire alle autorità nazionali “una pluralità di opzioni per soddisfare le loro esigenze quando progettano le strategie di vaccinazione”. Non potendo prevedere come il virus evolverà in futuro e quali varianti circoleranno quest’inverno, sono attualmente in fase di revisione da parte dell’Ema – o saranno presentati a breve – altri vaccini adattati che incorporano diverse varianti, come Omicron BA.4 e BA.5. Un supporto alla valutazione e all’autorizzazione arriverà proprio dai dati clinici generati attraverso i vaccini bivalenti originali/BA.1 raccomandati oggi.
‼️ EMA has recommended authorising the first adapted COVID-19 #booster vaccines.
The Comirnaty and Spikevax vaccines adapted to the Omicron BA.1 subvariant will provide broader protection against #COVID19.
➡️ https://t.co/6xcmoNRK5c pic.twitter.com/Lw7eqcG8dO
— EU Medicines Agency (@EMA_News) September 1, 2022
Il via libera dell’Ema era atteso da tempo dalla Commissione, che nel frattempo ha raggiunto un accordo con Moderna per la modifica dei calendari di consegna delle dosi di vaccini previste per l’estate (a partire da settembre), compresi quelli adattati alla variante Omicron una volta autorizzati. Dopo il parere positivo arrivato oggi, la commissaria europea per la Salute, Stella Kyriakides, ha annunciato che l’esecutivo comunitario procederà con “un’autorizzazione accelerata per garantire che possano essere introdotti rapidamente” in tutta l’Unione. Questi vaccini adattati potranno essere utilizzati “come dosi di richiamo che mirano al virus originale e alla sottovariante Omicron BA.1”, ha precisato Kyriakides, dal momento in cui “sono stati sviluppati per offrire una protezione maggiore e più ampia contro le varianti attuali e future”.
A questo si aggiunge anche l’attesa “nelle prossime settimane” del parere sui vaccini adattati Omicron BA.4 e BA.5, “nell’ambito dell’approccio al nostro ampio portafoglio di vaccini”, ha precisato la commissaria per la Salute: “Sono importanti per proteggere gli europei dal probabile rischio di ondate di infezioni autunnali e invernali, dobbiamo essere pronti ad affrontare un altro inverno con il Covid-19“. Anche considerato questo scenario, è arrivato da Bruxelles l’invito alle 27 capitali Ue a “pianificare e lanciare le campagne di vaccinazione” autunnali e invernali: “È essenziale continuare a dare priorità all’adozione della vaccinazione primaria e della prima dose di richiamo tra tutti gli individui idonei”, ha ricordato la commissaria Kyriakides, anticipando che l’esecutivo Ue presenterà “presto” una serie di “azioni per le strategie di vaccinazione contro il Covid-19” e “misure per evitare una nuova ondata” nei prossimi mesi. Anche se “la pandemia non è finita”, lo sviluppo e l’adattamento dei vaccini per rispondere al virus “è uno dei più grandi successi nella storia moderna della medicina”.
https://twitter.com/SKyriakidesEU/status/1565319161017950213?s=20&t=ziaISW536WGGQyfiS66I_A








![FAO G20 GREEN GARDEN AL PARCO DELLA CAFFARELLA GENDER EQUALITY UGUAGLIANZA DI GENERE. Caregiver Foto: [Imago economica]](https://www.eunews.it/wp-content/uploads/2026/05/Imagoeconomica_1577461-120x86.jpg)
